本篇目录:
- 1、有那几种标准电极电势?
- 2、汽车蓄电池国际标准有哪几种?
- 3、标准电池和工作电池的作用有何不同?
- 4、在标准状态下,用下列电对组成原电池,写出电池符号,电极反应和电池反应...
- 5、电极电势小于零说明什么
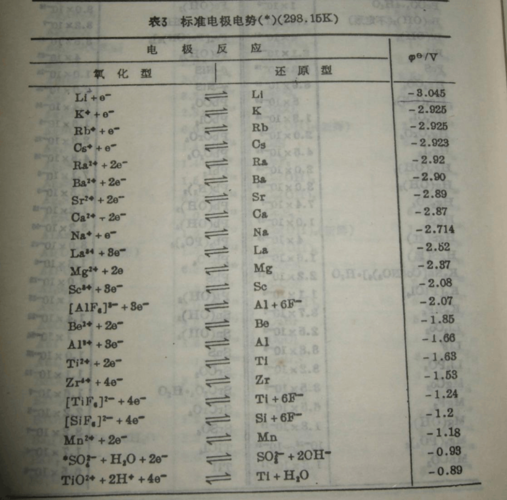
有那几种标准电极电势?
1、(l)一般采用电极反应的还原电势,每一电极的电极反应均写成还原反应形式,即:氧化型 + ne = 还原型; (2)标准电极电势是平衡电势,每个电对E值的正负号,不随电极反应进行的方向而改变。
2、标准值:0.2415V。饱和甘汞电极是一种运用电化学原理发明的道具,运用了饱和氯化钾溶液为电解液的甘汞电极25℃下的电极电势为0.2412V的特点而研制出来,在一般的化学生产中起着盐桥作用。

3、铜电极的标准电极电势是指参与电极反应的所有物质,气体必须是一个标准压强,溶液必须是一个标准浓度,其它固体、液体必须要纯净。所谓的铜电极是指以铜为材质制成的电极。
4、根据国际电化学委员会(IUPAC)发布的数据,铜的标准电极电势为+0.337 V。这个数值表示在标准状态下,铜电极与标准氢电极之间的电势差为+0.337 V。
5、对于该反应,电极电势(E)的能斯特方程为:其中ai是第i物种的活度,EA/B是A/B氧化还原对的标准氧化还原电位。后一个值与反应的标准吉布斯能直接相关。

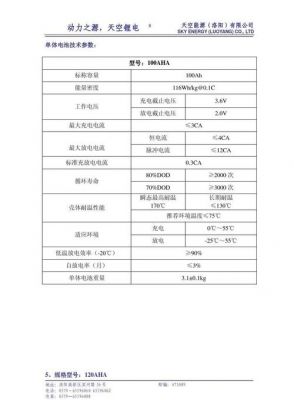
汽车蓄电池国际标准有哪几种?
汽车电池的类型有镍镉电池、镍氢电池、锂离子电池、锂聚合物电池和铅酸电池。
端柱类型共4种,分别为T1--细端柱、T2--粗端柱、ST--侧端柱和BT--螺纹端柱。近8成左右的汽车蓄电池,采用T2类型的粗端柱,而日本标准B系列蓄电池大多采用T1类型的细端柱。
汽车蓄电池类型有镍镉电池,镍氢电池,锂离子电池,锂聚合物电池,铅酸电。国家标准蓄电池以型号为6-QAW-54a的蓄电池为例,说明如下:6表示由6个单格电池组成,每个单格电池电压为2V,即额定电压为12V。

标准电池和工作电池的作用有何不同?
标准电极:在标准活度和标准压强下,随温度变化,电位稳定,极化小,可以作为标准测量对电极的点位及电位变化。工作电极:以测定请在铜电极上的反应极化曲线为例,工作电极(即研究电极)是发生析氢反应的场所。
工作电池的作用是提供补偿电压。标准电池用于确定R1的值,检测回路中流过电流是否为零。
工作电池:提供标准的工作电流。保护 (1)标准电池:不要振荡、严禁倒置、不可做电池用;(2)检流计:不用时将分流器置于“短路”档。
检流计:用于平衡直流电测量,如电桥中作为示零装置。标准电池:提供电动势的标准参考量,用以标定电位差计。工作电池:提供与待测电池电动势方向相反而数值几乎相等的外加电动势,用以对消待测电池的电动势。
标准电池指的是理论上,电阻忽略不计了,工作电池就有电阻了,电动势,电流都有变化。
在标准状态下,用下列电对组成原电池,写出电池符号,电极反应和电池反应...
1、左侧标有负极符号。在负极发生氢气被氧化成氢离子,其中以铂做催化剂,正极一侧铜离子被还原成铜单质。
2、正负号写在最两边,即“(-)”写在最左边,“(+)”写在最右边。里面一层一般写与外界导线相连的相。再里面一层写其他相。中间用双竖线“||”表示盐桥。相与相之间用逗号“,”或单竖线“|”分割。
3、由上例可见,任何一个自发进行的氧化还原反应原则上都可以组成原电池。
电极电势小于零说明什么
电极电势 E小于0,表明AgI转化为Ag不自发,而Ag/AgI的E则大于0,表明Ag可转化为AgI。
mol/L,或氢气压力小于101325Pa,电极电势就大于0,做正极,标准氢电极做负极。如果氢电极中氢离子浓度小于0mol/L或者压力大于101325Pa,电极电势小于零,做负极,标准氢电极做正极。这也叫浓差电池。
简单来说,这个反应本质上是氯气氧化二价氧生成氧气。但是氯气的氧化性不如氧气,自然不能应。其实就是这个反应的电极电势小于零,需要加入一个大于零的反应来使得总反应电极电势大于零,加入的就是更实惠的碳与氧气的反应。
这相当于第2条反应助推第1条反应的进行,这样总反应就可以发生了。若使用标准电极电势则使用:AgI + e = Ag + I(-)2H(+) + 2e = H2 前者的标准电极电势小于零,后者为零,所以反应也是可以进行的。
到此,以上就是小编对于原电池中标准状态是啥的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏