本篇目录:
HAc的解离度和标准解离常数的测量
根据测得的pH值,利用解离常数与pH值之间的公式计算Ka。具体的公式为:Ka=10^(-pH)/[H+]^2。其中,[H+]是氢离子的浓度。另外,醋酸的解离度也是一个重要的参数。它表示的是醋酸在溶液中解离的程度。
实验步骤:乙酸解离度和解离常数的测定 (1)配制不同浓度的乙酸溶液。用移液管分别量取已知浓度的HAc溶液00 mL、00 mL、200 mL于3只50mL容量瓶中,用蒸馏水稀释至刻度,摇匀。
醋酸溶液pH值的测定 用pHS-25型pH计,按醋酸浓度由稀到浓的次序测定1~5号HAc溶液的pH值,记录在表5-1中。 . 数据处理 计算表5-1中各项的值,计算出实验室温度时,HAc的解离常数,求算相对误差并分析产生的原因。
在测定醋酸的酸常数时,需要测定醋酸溶液的浓度,因为醋酸的酸常数是与其浓度相关的,即Ka=[H+][Ac-]/[HAc],其中[H+]表示氢离子浓度,[Ac-]表示醋酸根离子浓度,[HAc]表示醋酸的浓度。
值,根据 pH== - lg[H 3 O + ] 计算出来。 [ HAc ] = C HAc - [H 3 O + ] ,而 C HAc 可以用 NaOH 标准溶液通过滴定测得。这样,便可计算出该温度下的 K a ,进而也可求得醋酸的解离度α。

HAc为一元弱酸,在水溶液中存在如下解离平衡。HAc=H++Ac- Ka。起始浓度(molL-1) c 0 0。平衡浓度(mol?L-1) c–cαcαcα。Ka表示HAc的解离常数,α为解离度,c为起始浓度。
如何测定HAc的解离度和解离常数?
1、实验目的了解用pH法和电导率法测定醋酸解离度和解离常数的原理和方法。加深对弱电解质解离平衡的理解。 学习pH计和电导率仪的使用方法,练习使用移液管。
2、准备一定浓度的醋酸溶液,例如0.1M。使用pH计测定该醋酸溶液的pH值。根据测得的pH值,利用解离常数与pH值之间的公式计算Ka。具体的公式为:Ka=10^(-pH)/[H+]^2。其中,[H+]是氢离子的浓度。

3、.醋酸溶液pH值的测定 用pHS-25型pH计,按醋酸浓度由稀到浓的次序测定1~5号HAc溶液的pH值,记录在表5-1中。 . 数据处理 计算表5-1中各项的值,计算出实验室温度时,HAc的解离常数,求算相对误差并分析产生的原因。
4、醋酸标准解离常数和解离度的测定如下:实验目的 学习并掌握醋酸电离度和电离常数的测定方法;进一步练习滴定及溶液配制的操作;学习使用酸度计。
5、醋酸解离平衡常数的测定实验目的1.掌握弱酸的解离度和解离平衡常数的测定方法;2.掌握用pH计测定溶液pH的方法;3.熟悉酸碱滴定法测定HAc溶液浓度。
食用白醋中HAc浓度的测定方案
1、用25mL移液管移取50mL稀释后的白醋于250 mL锥形瓶中,加入2 d酚酞指示剂,摇匀,用已标定的NaOH标准溶液滴定至溶液呈微红色,30秒内不褪色,即为终点。 平行测定三份,计算白醋中醋酸的含量(g/100 mL)。
2、公式:X%(HAC)=C(NaOH)×V(NaOH)×M(HAC)×100/(1000×V×d)X % 表示食醋中总酸的百分浓度;C(NaOH)表示用来滴定的氢氧化钠的浓度,单位:mol/l;V(NaOH)表示滴定消耗的氢氧化钠溶液的体积。
3、实验目的:通过醋酸的电位消定,掌握电位消定的基本操作、PH的变化及指示剂的选择。学习食用醋中醋酸含量的测定方法。实验原理:食用的主要酸性物质是醋酸(HAC),此外还含有少量其他的弱酸。
测定hac溶液的ph时,为什么按由稀到浓的次序进行
弱电解质的电离常数在一定温度下是个定值,在测定时要排除温度干扰(浓溶液电离放热明显),依浓度梯度递减分多组来做,最后取平均值,这样可使实验数据更加精确。
若是先测量浓度高的溶液形成的高电势对测量低浓度溶液有较大影响,形成较大误差。先测浓度低的,再测浓度高的则误差可忽略不计。
因为浓度大的溶液会影响酸度计测量时的灵敏度,从而造成PH值不精确。稀释的溶液更容易得到精确的PH值。
测定ph值时,要按从稀到浓的次序进行是为了降低相对误差。测同一种溶质的溶液时,两组测量之间是不会洗PH计的电极的,所以会把前一种溶液的残留带入后一种。
这只是一种测试方法而已,也可以从浓到稀,只要你可以每测试一次就清理容器重新配比,或者适当添水,前提是你有足够大的容器(99%浓度稀释成1%需要增加溶剂9900倍),而且你还需要足够的溶质可以用。
怎样测量食醋的总酸度?
1、食醋中含醋酸大约为3%~5%,浓度较大,需要稀释。如果食醋的颜色较深,必须加活性炭脱色,否则影响终点观察。取10mL食醋样品,定容于250mL容量瓶中。食醋总酸度的测定。
2、计算总酸量:根据滴定的结果计算出每毫升氢氧化钠相当于的醋酸量,再乘以样品体积,即可得到食醋中的总酸量。注意事项 实验过程中要保证玻璃器皿的清洁度,避免误差的产生。
3、(2)总酸的测定 称吸取10mL醋样于100mL容量瓶中,加水稀释到刻度,定容。
4、实验步骤 食用醋总酸度的测定 准确吸取食用醋试样0mL置于100mL容量瓶中,加水稀释至刻度,摇匀。
5、总酸是指最终能释放出的氢离子数量,是一个定数;PH代表物质在溶液中释放氢离子(或氢氧根)的能力,涉及到一个溶液中H+的平衡问题,可以随物质的浓度变化而释放或多或少的H+。本方法适用于食醋中总酸的现场快速检测。
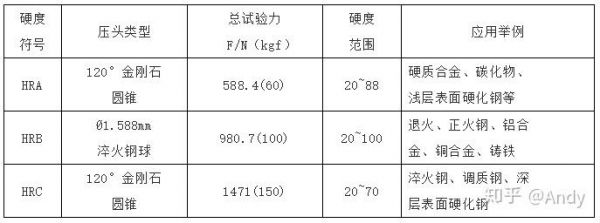
到此,以上就是小编对于hrc测试范围的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏